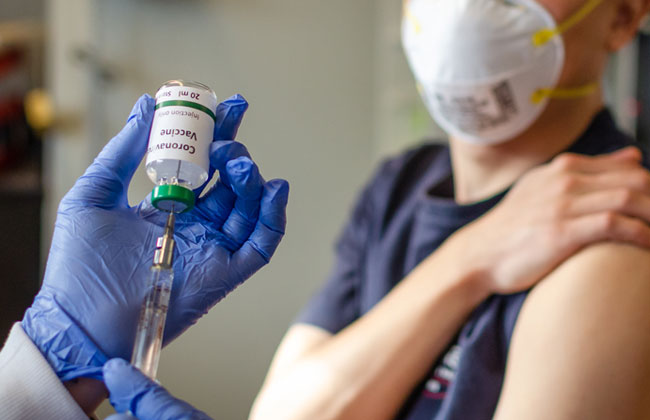
Der französisch-britische Impfstoff der Pharmakonzerne Sanofi und GSK liefert laut Studie vielversprechende Ergebnisse. Er könnte im Kampf gegen Mutationen eine große Rolle spielen.
Gute Nachrichten im Kampf gegen die Corona-Pandemie: Der Impfstoffkandidat von Sanofi und GlaxoSmithKline (GSK) hat laut den Herstellern in Studien der Phase II eine gute Wirksamkeit gezeigt. Die Vakzine löste in allen Altersgruppen eine starke Immunantwort aus. Die Studienphase III, die für die Zulassung entscheidend ist soll schon kommende Woche beginnen. Mit der endgültigen Zulassung rechnen die Hersteller noch dieses Jahr.
Neuartiger Impfstoff
Anders als die bisher in der EU zugelassenen Impfstoffe handelt es sich bei dem nun getesteten Produkt um eine proteinbasierte Vakzine. Diese haben den Vorteil, dass sie nicht so kühl gelagert werden müssen und in großen Mengen hergestellt werden können. Zudem könnten sie als mögliche Drittimpfungen zur Auffrischung gegen neu auftretende Virusvarianten fungieren.
Auffrischung gegen Mutanten?
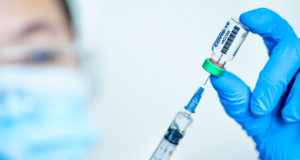
Der Impfstoffkandidat von Sanofi basiert auf derselben Technologie, die der Konzern bereits bei seinem Grippeimpfstoff einsetzt. Der Impfstoff gegen das Coronavirus enthält ein typisches Eiweiß, das sogenannte Spike-Protein. Das Protein wird mithilfe spezieller Viren hergestellt, die in den Zellen von Insekten heranwachsen. Neben dem Spike-Protein enthält die Impfung noch einen Wirkverstärker des britischen Pharmakonzerns GSK. Das Spike-Protein allein ist ungefährlich. Das Immunsystem erkennt den Eindringling jedoch und bringt Abwehrkräfte in Stellung, die vor einer Infektion mit dem echten Coronavirus schützen sollen.

Phase-II-Studie zeigt hohe Wirksamkeit
An der aktuellen Studie der Phase II hatten 722 Freiwillige zwischen 18 und 95 Jahren in den USA und Honduras teilgenommen. Die Ergebnisse der Untersuchung zeigten, dass Probanden aus allen Altersgruppen nach der zweiten Dose des Impfstoffs ähnlich viele Antikörper entwickelten wie Menschen, die an Covid-19 erkrankt waren. Die Immunantwort bei den 18- bis 59-Jährigen viel höher aus als beim Rest. In dieser Phase II wurden die Wirksamkeit des Impfstoffs bei der Verhinderung der Krankheit und die geeignete Dosierung getestet.
Bei Probanden, die sich bereits mit dem Coronavirus infiziert hatten, ließ sich zudem schon nach einer Dosis eine hohe Antikörperzahl nachweisen. Die Impfung könnte deshalb auch als Auffrischung eingesetzt werden, so die Hersteller.
Studie mit 35.000 Probanden geplant
Für eine Zulassung ist eine weitere Studie der Phase III notwendig. Dabei werden die Wirksamkeit, die Sicherheit sowie die Dosierung der Impfung bestätigt. Außerdem sollen in dieser Phase unerwünschte Ereignisse, wie etwa ein besonders schwerer Krankheitsverlauf durch die Impfung, ausgeschlossen werden. Für diese Phase ist eine Studie mit 35.000 Probanden geplant. Dabei sollen zwei Varianten der Impfung getestet werden:
- eine, die sich gegen die ursprüngliche Variante des Virus richtet
- und eine gegen die südafrikanische Virus-Variante B.1.351. Laut ersten Studien sind bereits zugelassene Impfungen weniger wirksam gegen B.1.351.
Zudem soll in weiteren Studien geprüft werden, ob der Impfstoff von Sanofi als Auffrischung gegen neue Virusvarianten wirksam sein könnte, egal mit welchen Vakzinen die Betroffenen zuvor geimpft wurden.
Impfstoff kommt deutlich später als erhofft
Die Europäische Union hatte große Hoffnungen in den proteinbasierten Impfstoff gesetzt und bereits im September ein Abkommen mit Sanofi geschlossen, um sich 300 Millionen Dosen für die EU zu sichern. Allerdings gab es Probleme mit falschen Messwerten, weshalb die Studien der Phase II wiederholt werden mussten.
Damit der Impfstoff nun möglichst schnell zur Verfügung steht, soll er bereits produziert werden, ehe die Studienphase III abgeschlossen ist – auch auf die Gefahr hin, dass er niemals eingesetzt wird. Sanofi und GSK hoffen jedoch, dass der Impfstoff noch Ende 2021 zugelassen werden kann.
Quellen und Links:
Folge uns auf Social Media!